ついに。
iPS細胞を使った再生医療製品、世界初の正式承認――日本発の医療技術が実用化へ
ニュースの概要
2026年3月6日、上野厚生労働大臣は、iPS細胞(人工多能性幹細胞)を用いた再生医療製品2品目の製造・販売を、条件付きで正式に承認した。iPS細胞由来の再生医療製品が国家承認を受けるのは世界で初めてのことである。
承認されたのは以下の2製品。
ひとつは、大阪大学発のベンチャー企業「クオリプス」が開発した心不全患者向けの心筋シート「リハート」。もうひとつは、製薬会社「住友ファーマ」が開発したパーキンソン病患者向けの細胞治療製品「アムシェプリ」。
両製品はいずれも、2026年2月に厚労省の専門部会が「今後7年間にわたってさらに有効性を検証すること」などを条件として製造・販売を了承していた。今回の正式承認により、次のステップである薬価(保険適用価格)の決定などの手続きに移行する。早ければ2026年夏にも、患者が実際に治療を受けられる見通しだ。
要点
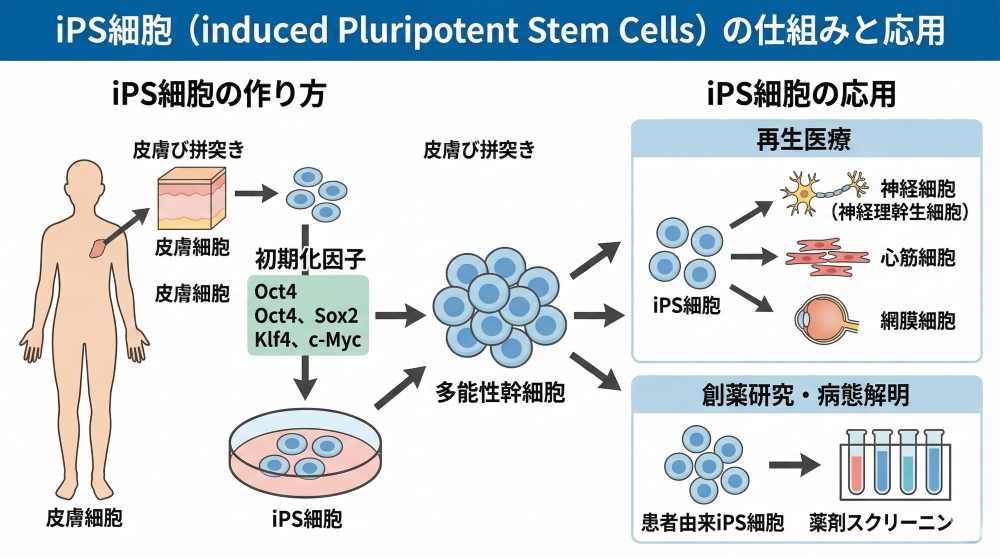
①世界初の快挙 iPS細胞技術は、2006年に京都大学の山中伸弥教授(現・特別教授)が樹立に成功し、2012年にノーベル生理学・医学賞を受賞した日本発の技術。今回の承認により、その技術が実際の治療製品として世界で初めて実用化されることになった。
②対象疾患は「心不全」と「パーキンソン病」 心不全は日本国内だけでも患者数が100万人超とされる重篤な疾患。パーキンソン病も根本的な治療法が乏しく、患者・家族の負担が大きい難病だ。既存の治療では対応が難しい患者層への新たな選択肢となる可能性がある。
③「条件付き承認」という枠組み 今回の承認は「条件付き」であり、製品を販売しながら7年間にわたって有効性・安全性のデータを引き続き収集・検証することが義務づけられる。これは日本の薬事制度における「条件及び期限付き承認」の仕組みで、有望な再生医療製品を早期に患者に届けるための制度である。完全な有効性の証明を待たずに承認するため、スピードと安全性のバランスをどう確保するかが課題として残る。
④産学連携モデルの成果 クオリプスは大阪大学の研究を起点に設立されたベンチャー企業であり、住友ファーマは大手製薬会社。大学の基礎研究がベンチャーや製薬企業との連携を通じて製品化に至った点は、今後の再生医療分野における産学連携モデルの先例となりうる。
争点・論点
◆「条件付き」でよいのか――有効性・安全性の不確かさ 最も大きな論点は、長期的な有効性と安全性がまだ完全には確認されていない段階での承認の是非だ。7年間のデータ収集が義務とはいえ、その間に患者が治療を受けることになる。iPS細胞由来の製品はがん化リスクなどの懸念も指摘されており、承認後の監視体制の実効性が問われる。
◆薬価はどうなるか――医療費への影響 再生医療製品は製造コストが極めて高く、薬価が高額になる傾向がある。過去には別の再生医療製品が保険適用後に高額な薬価をめぐって議論を呼んだ事例もある。今回の2製品についても、保険収載後の薬価設定と費用対効果の評価が焦点になる。
◆日本の「条件付き承認制度」の国際的評価 欧米の規制当局と比べ、日本は再生医療製品に対して比較的早期の承認を認める制度設計をとっている。これを「患者への迅速なアクセスを実現する先進的な制度」と評価する見方がある一方、「エビデンスが不十分なまま実用化を急ぎすぎる」との批判も根強い。世界初の実用化という実績が、国際標準のあり方にどう影響するかも注目点だ。
◆今後の再生医療市場への波及 今回の承認が呼び水となり、iPS細胞を使った他の疾患向け製品の開発・承認申請が加速するとみられる。脊髄損傷や網膜疾患など、国内外で臨床試験が進む領域も多く、産業・医療の両面でその動向が注目される。

今回のニュース、読んでいて「ついにきたか」と思いました。
iPS細胞といえば、山中先生のノーベル賞受賞で日本中が湧いたあの技術ですよね。あれから13年、「すごい研究だけど、自分の生活にはまだ遠い話」という感覚がずっとありました。それが今回、心不全やパーキンソン病の患者さんが実際に治療を受けられるところまで来たわけです。これは本当に大きな一歩だなと思います。
個人的に注目しているのは、大阪大学発のベンチャー企業がここまでたどり着いたという点です。大学の研究室で生まれたアイデアが、ベンチャーという形で育って世界初の製品承認へ——日本でもこういうストーリーが実現できるんだ、という事実は素直に嬉しいですね。
「条件付き承認」という点を気にする声があるのも分かります。7年間の検証が続くという意味では、まだ旅の途中ではあります。ただ、「治療の選択肢がある」ことと「ない」ことの差は、当事者にとっては計り知れないものがあるはず。一刻も早く届けたいという姿勢を、私は前向きに受け止めたいです。
薬価や医療費など、これから議論すべきことはまだ残っています。でも今日くらいは、日本発の技術が世界を先導したという事実をシンプルに喜びたいと思います。今年の夏、最初の患者さんが治療を受ける日が来るかもしれない——その日が楽しみです。



















コメント